بیماری آلزایمر می تواند در موارد نادری در نتیجه اقدامات پزشکی بین افراد منتقل شود. این کشف پس از یک یک تحقیق بیماران غیرعادی جوان آلزایمر در بریتانیا، که همه آنها در کودکی هورمون رشد دریافت کرده بودند.
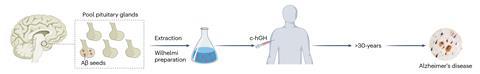
این هورمونها از غدد هیپوفیز افراد متوفی میآیند، روشی که در سال 1985 به دلیل ارتباط آن با انتقال پروتئینهای تاخورده اشتباه – پریونها – که باعث بیماری کروتزفلد-جاکوب (CJD) میشوند، ممنوع شد.
بین سالهای 1959 تا 1985، حداقل 1848 بیمار با هورمون رشد انسانی از غده هیپوفیز انسان درمان شدند که منجر به بیش از 200 مورد CJD شد که 80 مورد آن فقط در بریتانیا بود. اکنون به نظر می رسد که این روش افراد را در معرض خطر ابتلا به بیماری آلزایمر نیز قرار می دهد. گروه تحقیقاتی بریتانیایی پشت این کار همچنین هشدار داد که احتمالاً هورمون رشد بیشتری نسبت به پریون های CJD با آمیلوئید بتا آلوده می شود و دوره نهفتگی آلزایمر نسبت به CJD طولانی تر است.
اولین اشاراتی مبنی بر اینکه بیماری آلزایمر تحت شرایط بسیار خاص منتقل می شود، زمانی بود که دانشمندان علوم اعصاب از دانشگاه کالج لندن (UCL) مغز هشت فرد مبتلا به CJD اکتسابی پزشکی را بررسی کردند. ناگهان دیدند نشانه های آلزایمر بیماری به شکل تودههای پروتئین بتا آمیلوئید یا پلاکهای آمیلوئید در ماده خاکستری – نشانهای از این بیماری پیشرونده مغزی است.
ظن محققان UCL با این واقعیت تأیید شد که بافت مغز آلزایمر انسان می تواند پلاک های بتای آمیلوئید را در مغز موش ایجاد کند. در سال 2018، تیم گروه های ذخیره شده هورمون رشد استخراج شده از غدد هیپوفیز و نشان داده شده که می توانند پلاک های آمیلوئید بتا را در موش بکارند.
هشت بیمار که دچار اختلال شناختی شدند به کلینیک ملی پریون در لندن ارجاع شدند و پنج نفر از آنها علائمی مطابق با بیماری آلزایمر نشان دادند. کالبد شکافی یکی از دو بیمار که در طول مطالعه جان خود را از دست دادند نشان داد که آنها علائم بیماری آلزایمر را دارند.
پنج نفری که به آلزایمر مبتلا شدند، میگوید: «کمی با آنچه شما ممکن است آلزایمر کلاسیک بنامید متفاوت بودند». جان کولینگ، عصب شناس دانشگاه UCL که این مطالعه را رهبری کرد. او می افزاید که این تعجب آور نیست، زیرا هورمون های رشد آلوده راه بسیار متفاوتی برای ایجاد این بیماری هستند.
میگوید: «تعداد کمی از افراد است، اما قابل توجه است که آسیبشناسی آمیلوئید آنها شبیه آلزایمر در مراحل اولیه است، اما شما آسیبشناسی تاو زیادی را مشاهده نمیکنید». پل مورفی، محقق آلزایمر در دانشگاه کنتاکی. او توضیح میدهد که تصور میشود که تاو پلاکهای آمیلوئید را دنبال میکند و بسیاری از نورونها را میکشد، که سپس باعث مشکلات شناختی میشود.
بیشتر بیماری آلزایمر به طور ناگهانی بروز می کند و بیماران پس از 65 سالگی علائم را نشان می دهند. شکل دوم می تواند در اوایل زندگی در نتیجه جهش های ژنتیکی خاص ظاهر شود. این مطالعه جدید به سومین شکل اکتسابی آلزایمر اشاره می کند.
کولینگه میگوید: «شما میتوانید این موارد بسیار نادر را داشته باشید، درست مانند CJD، که در آن افراد بهطور تصادفی در نتیجه یک روش پزشکی در معرض این دانههای قابل انتقال قرار میگیرند». “بیشتر این به روش های پزشکی مربوط می شود که دیگر استفاده نمی شود.”
برای CJD، این شامل پیوند غشای مغز برای ترمیم نقایص در طول جراحی مغز و اعصاب و پیوند قرنیه، و همچنین از طریق ابزارهای جراحی آلوده است. بیشتر CJD به صورت پراکنده یا از طریق جهش های ارثی رخ می دهد که حدود 1٪ تخمین زده می شود که اکتسابی باشد.
محقق بیماری آلزایمر بارت دی استروپ در UCL، که در مطالعه جدید شرکت نداشت، میگوید که افزایش هوشیاری ضروری است، بهویژه در مورد روشهای در سنین پایین که شامل مایعات یا بافتهای انسانی است. او پیشنهاد میکند که از نزدیک آنچه را که برای گروههایی از بیمارانی که روشهایی مانند انتقال خون یا پیوند اعضا انجام میدهند، روی میدهد. او خاطرنشان می کند: «این چیزی است که ما بیش از همه به آن نیاز داریم تا بفهمیم مشکل چقدر بزرگ است. “در این مرحله به نظر یک اتفاق بسیار نادر است.”
کالینگ همچنین هشدار می دهد که تحقیقات آنها نشان می دهد نتایج دلگرم کننده درمان های آنتی بادی مونوکلونال برای بیماری آلزایمر ممکن است زودرس باشد ما می دانیم که در بیماری پریون، اگر دارویی تولید کنید که به اکثر اجزای سویه زمینه ای متصل شود. [of prion] که به مغز گسترش می یابد، می توانید رشد سریع مقاومت را از گونه های ثانویه موجود دریافت کنید.
مورفی این ایده را “جذابکننده” مینامد، اما میگوید به نظر میرسد نوعی پروتئین بتا آمیلوئید وجود دارد که بهویژه در بیماری آلزایمر مضر است و هر درمانی که بتواند بهقدر کافی از شر آن خلاص شود، باید برای بیماران تفاوت ایجاد کند.